MFN1(Mitofusin 1)作为线粒体外膜融合的关键调控蛋白,已被证实在雄性小鼠精原细胞分化及雌性小鼠卵泡发育中发挥重要调控作用。然而,MFN1在植入前胚胎发育过程中的具体功能,以及其与表观遗传重编程的潜在关联尚未得到充分阐释。本研究旨在探究MFN1在小鼠植入前胚胎发育中的生物学功能及其分子作用机制。
2025年3月 日17日,华中科技大学同济医学院周立全/何西淼/马冰馨在Advanced Science杂志上发表题为“Mitofusin 1 drives preimplantation development by enhancing chromatin incorporation of histone H3.3”的研究论文。该研究通过显微注射技术结合IP-MS、co-IP、转录组测序及ChIP-seq测序,阐明了线粒体融合蛋白MFN1调控小鼠早期胚胎发育的新机制,揭示了MFN1除参与线粒体动力学调控外,还与细胞质晶格蛋白形成复合物,并通过影响组蛋白H3.3的表达来调节早期胚胎的表观遗传修饰。
在本研究中,团队首先对免疫荧光染色结果及小鼠卵母细胞和早期胚胎转录组和翻译组数据进行联合分析鉴定出MFN1在卵母细胞成熟和早期胚胎发育进程中持续表达。MFN1缺失会引发一系列发育异常表型,包括:GV期卵母细胞中MFN1缺失导致卵母细胞成熟障碍;减数分裂过程中MFN1缺失影响受精后雄原核形成;MII期卵母细胞中MFN1缺失引起受精后合子基因组激活(ZGA)活性下降且胚胎发育阻滞于2细胞期;而合子期MFN1缺失则导致早期胚胎发育停滞在桑椹胚阶段。这些结果表明MFN1在小鼠早期胚胎发育中具有重要的生物学功能。
为进一步探究MFN1调控原核形成及早期胚胎发育的机制,团队采用免疫共沉淀-质谱串联(coIP-MS)鉴定出MFN1与细胞质晶格组分PADI6有相互作用。细胞扩展后染色实验也显示MFN1与PADI6在卵母细胞中具有较强的共定位。结合H3.3敲低实验,团队进一步证实,MFN1缺失通过破坏细胞质晶格结构和核糖体蛋白亚基组装影响蛋白质翻译活性,最终导致对翻译活性敏感的组蛋白H3.3表达水平下降和雄原核形成障碍。
接下来,结合H3.3敲低实验以及微量细胞转录组测序、ChIP-seq测序和分析,发现MFN1缺失导致染色质上H3.3富集显著减少。关于染色质分布的分析结果显示,H3.3在基因组上的定位与RNA聚合酶II以及活性组蛋白修饰H3K27ac富集水平呈正相关。而MFN1缺失和H3.3缺失后胚胎基因组上RNA聚合酶II和H3K27ac的分布明显减弱。上述结果表明,MFN1通过介导H3.3在活性转录基因转录起始位点处的沉积,促进早期胚胎基因转录活性。
最后,团队发现MFN1小分子激动剂S89的补充可显著改善母源衰老小鼠早期胚胎中的线粒体功能并提高H3.3蛋白表达水平,从而促进早期胚胎的发育。此外,团队还发现在人类早期胚胎中,MFN1蛋白表达水平与H3.3蛋白表达水平呈正相关,且二者表达水平均随年龄增长而显著降低,为解析年龄相关的早期胚胎发育缺陷提供了新的研究思路,具有潜在的生殖临床应用价值。
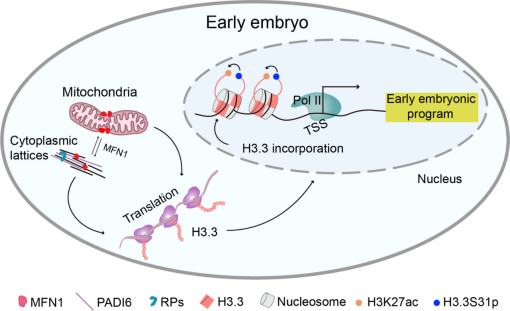
综上所述,该研究首次提出了MFN1在小鼠早期胚胎发育中调控线粒体和细胞质晶格的功能,促进组蛋白H3.3在早期胚胎染色质上的掺入,确保原核正常形成和2细胞期胚胎顺利发育,并维持早期胚胎发育程序的精确调控。该研究揭示了MFN1在小鼠植入前胚胎发育过程中非经典线粒体融合功能及其参与表观遗传重编程的分子机制,同时也为MFN1表达缺失可能介导年龄相关人类胚胎发育缺陷的临床研究提供了新的视角。
华中科技大学同济医学院生殖健康研究所周立全教授、基础医学院何西淼教授、以及附属同济医院马冰馨副研究员为该论文的共同通讯作者。华中科技大学同济医学院生殖健康研究所2021级博士研究生时小燕为该论文的第一作者。课题组博士研究生田雨、硕士研究生王宇帆、博士研究生张奕然对本研究亦有重要贡献。该课题得到了国家自然科学基金项目和华中科技大学学术前沿青年团队支持计划的资助。(通讯员 时小燕)

 官方微信公众号
官方微信公众号